门诊管理软件注册申报|道和思源CRO代办公司
日期:2020-05-07 / 人气: / 来源: / 编辑:Sasha大家都知道,软件是没有物理实体的,它是一系列按照特定顺序组织的计算机数据和指令的集合。一般来讲软件被划分为系统软件、应用软件和介于这两者之间的中间件。软件并不只是包括可以在计算机上运行的电脑程序,与这些电脑程序相关的文档一般也被认为是软件的一部分。而门诊管理软件就是“软件”的一种。门诊管理软件按字面理解,就是供医疗行业使用的软件。比如有医院管理系统、区域卫生信息平台、设备科专用管理软件、出入境体检及预防接种软件、健康体检软件、检验系统软件、数字医学影像、药品及收费软件、电子病历软件、基层医疗管理软件、健康管理软件、医疗信息交换软件、健康信息转储发布等。

当一个公司把医疗软件开发出来,想要运用到医院的时候,是必须进行门诊管理软件注册申报的,也就是行业说的门诊管理软件注册证。然而因为门诊管理软件注册申报是涉及到相关法律法规的,甚至有的需要做临床的,所以,还是需要有对应的专业人员来操作。这时候大部分公司都会把门诊管理软件注册申报的项目外包出去,找一些门诊管理软件注册代办公司来做。
道和思源,全名道和思源(北京)科技有限公司,公司成立于2014年,专注于医疗器械法规咨询服务,致力于为客户将安全、有效和合规的医疗器械产品迅速推向并占领全球市场,是中国领先的医疗器械CRO创新服务企业。道和思源秉承效率就是生命的原则,首创X7省时系统等创新服务,公司主要代办国家药监局NMPA业务有:进口一类医疗器械备案、进口二类医疗器械注册、进口三类医疗器械注册、国产北京一类医疗器械备案、国产二类医疗器械注册、国产三类医疗器械注册、门诊管理软件注册、AI人工智能医疗软件注册、人类体外辅助生殖技术用液注册。公司为Dignoptics Technologies B.V、Advanced Back Technologies, Inc、GN OTOMETRICS A/S、Duerr DENTAL AG等包括中国企业在内的近百家企业提供了医疗器械临床试验注册等高效服务,项目平均省时超过60天,赢得了广大企业的良好口碑,连续多年被客户赞为值得信赖的法规咨询供应商。
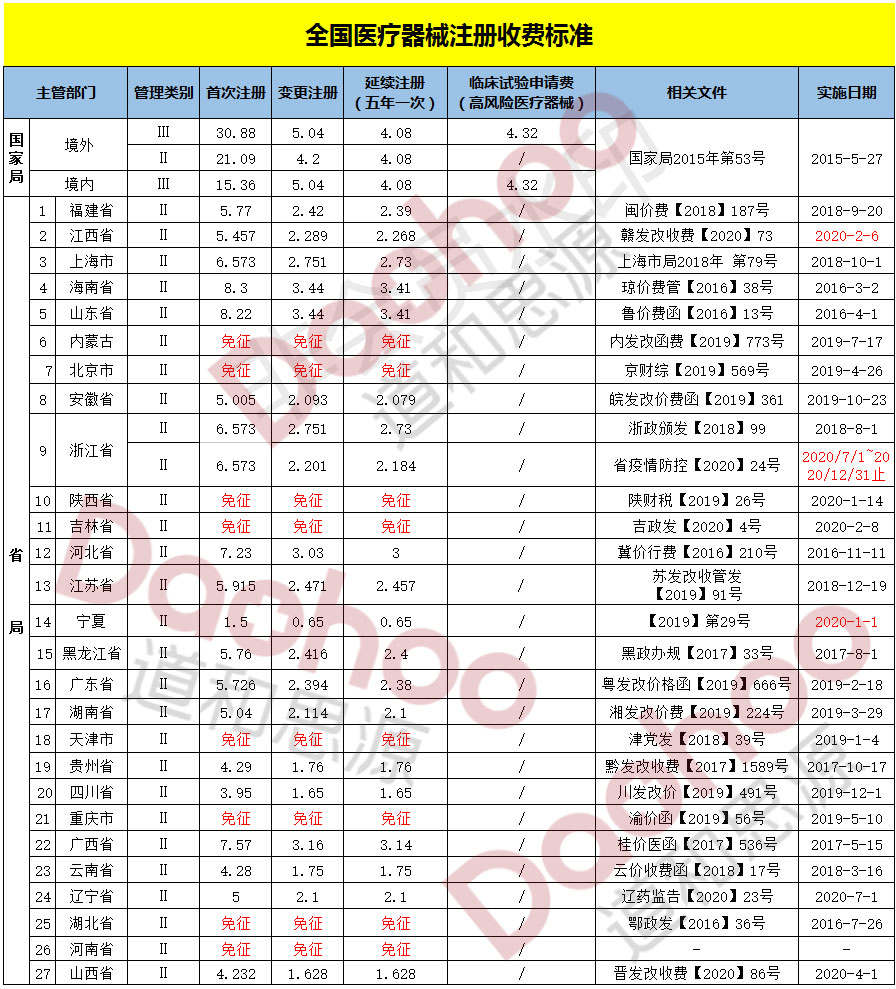
医疗器械收费表
门诊管理软件注册申报相关知识
1、门诊管理软件注册申报涉及的相关法律法规
1.门诊管理软件注册技术审查指导原则
用于指导企业提交门诊管理软件注册申报资料,同时规范门诊管理软件的技术审评要求。指导原则在现行法规要求下进一步明确了对门诊管理软件的要求,特别是对软件更新、软件版本升级明确了具体要求。指导原则包括范围、基本原则、软件描述文档、软件更新、软件版本、现成软件、注册申报资料要求等内容,并将独立软件产品技术要求模板作为附录列出。关于软件更新,指导原则明确,门诊管理软件发生重大软件更新应进行许可事项变更,而发生轻微软件更新通过质量管理体系进行控制,无需进行注册变更,待到下次注册(注册变更和延续注册)时提交相应申报资料。
2.移动医疗器械注册技术审查指导原则
该指导原则适用于采用无创“移动计算终端”实现一项或多项医疗用途的设备和/或软件。明确了移动医疗器械的定义、类型、判定原则和注册申报资料总体要求。该指导原则应结合《门诊管理软件注册技术审查指导原则》、《医疗器械网络安全注册技术审查指导原则》和相关医疗器械产品注册技术审查指导原则的要求进行使用。
根据指导原则要求,移动医疗器械作为移动计算技术与传统医疗器械的结合,除考虑传统医疗器械的要求之外还需综合考虑移动计算技术的特点、风险及其控制措施,包括网络安全能力、显示屏限制、环境光影像、电池容量限制、云计算服务等。

2、门诊管理软件注册申报要不要做分类检定的要求
如果你申报的门诊管理软件不在一二三类栏目了,就要去做医疗器械的分类检定。或者也可以看下符不符合申报创新医疗器械。
3、医疗器械监督管理条例
对规范医疗器械研制、生产、经营、使用活动,加强医疗器械监督管理,保障医疗器械安全有效、促进产业发展起到了积极作用。
4、医疗器械注册管理办法
医疗器械注册是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其结果进行系统评价,以决定是否同意其申请的过程。医疗器械备案是由医疗器械备案人向食品药品监督管理部门提交备案资料,由食品药品监督管理部门对提交的备案资料存档备查。为规范医疗器械的注册与备案管理,保证医疗器械的安全、有效,根据《医疗器械监督管理条例》,国家食品药品监督管理总局局务会议审议通过并制定下发了《医疗器械注册管理办法》。在中华人民共和国境内销售、使用的医疗器械,应当按照本办法的规定申请注册或者办理备案。医疗器械注册与备案应当遵循公开、公平、公正的原则。
温馨提示,本站部分内容来源网络,如有侵权,请联系删除!

道和思源(北京)科技有限公司成立于2014年,专注于医疗器械法规咨询服务,致力于为客户将安全、有效和合规的医疗器械产品迅速推向并占领全球市场,是中国领先的医疗器械CRO创新服务企业。主要服务项目有:进口一类医疗器械备案、进口二类医疗器械注册、进口三类医疗器械注册、国产三类医疗器械注册、医疗器械软件注册、临床实验、创新医疗器械申报港澳台医疗器械注册等。
猜你喜欢
- 医疗器械技术审评补正资料预审查服务2018-12-10
- 山西运城开展无菌和植入性医疗器械监督检查2020-11-16
- 安徽省推进实施医疗器械唯一标识(UDI)工作方案2022-05-18
- 医疗器械安全和性能基本原则符合性技术指南使用说明2022-07-14
- 国家药监局公布经导管人工肺动脉瓣膜系统获批上市2022-07-12
- 吉林省药监局通化检查分局开展疫情防控用医疗器械重点产品检查2020-06-11
- 创新医疗器械特别审查申请审查结果公示(2020年第19号)2020-11-04
- 国家药监局关于发布国家医疗器械监督抽检结果的通告2019-10-17
- 器审中心6月22日发布《药物涂层球囊扩张导管注册审查指导原则(征求意见稿)》2022-06-23
- 2019年3月进口第一类医疗器械产品备案信息2019-04-04
- 河南省药监局发布2021年第5期对医疗器械抽查不合格处置通告2021-12-01
- 国家卫健委等十部委印发通知,药物Dextenza获得美国FDA批准2018-12-06
- 新疆维吾尔自治区药监局党组书记张钰祥带队调研伊犁州防护用品生产企业2020-06-28
- 国家药监局发布63项医疗器械行业标准的公告2021-09-10
- 与国际接轨!医疗器械临床试验默许制来了!2019-04-04
- 企业系统管理软件注册申报|道和思源CRO代办公司2020-05-07